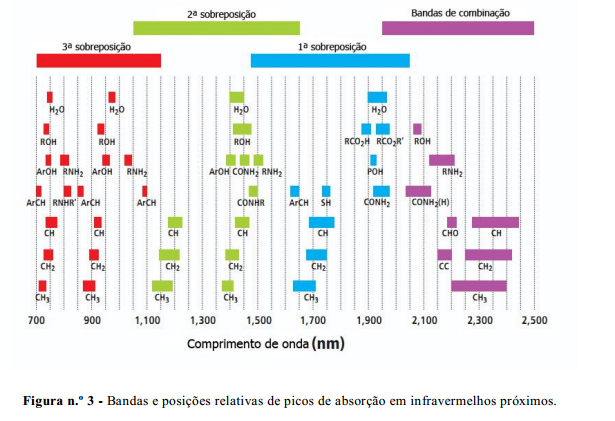
Espectroscopia por refletância difusa no infravermelho com transformada de Fourier
Espectroscopia por refletância difusa no infravermelho com transformada de Fourier
A
espectroscopia por refletância difusa é principalmente observada em
amostras sólidas pulverizadas, sendo sua aplicação prática muito
difundida na literatura, podendo ser utilizada em equipamentos que
operam na região do infravermelho próximo (Blanco et al., 2001; Pasikatan et al., 2003; Pasquini, 2003, Steuer, Schulz, 2003; Sun, Xiang, An, 2004), associada a sigla NIRRS, Near Infrared Reflectance Spectroscopy,
ou simplesmente NIRS. No final dos anos 70 e início dos 80 foi
demonstrada a utilidade deste fenômeno quando acessórios de
refletância difusa foram acoplados com espectrômetros
interferométricos com transformada de Fourier (DRIFTS) (Fuller,
Griffths, 1978).
A
refletância difusa é observada quando uma luz incide em uma matriz
descontínua, penetra na amostra (amostras do tipo pó, sólido, placa
ou filme) e reflete trazendo informações espectrais. O caminho
percorrido pela luz no interior da matriz pode ser considerado
aleatório devido a múltiplas reflexões, algumas das quais após
percorrer o interior de algumas partículas que constituem a amostra.
Desta forma a luz refletida pode ser atenuada por absorção e o
espectro resultante é similar ao obtido através da técnica no
infravermelho por transmissão utilizando KBr (brometo de potássio).
Uma importante diferença entre a transmissão e a refletância se dá
devido o diferente caminho óptico percorrido pela luz. Enquanto que
na transmissão o caminho óptico é constante para todo número de onda,
na refletância por sua vez, o caminho pode ser variável. É de
conhecimento geral que em regiões do espectro, onde a amostra absorve
fracamente, a luz penetra mais profundamente na matriz, sendo que o
contrário acontece onde há forte absorção. Portanto, ao se comparar o
espectro obtido por transmissão (pastilha de KBr) com o obtido por
refletância, as intensidades relativas das bandas serão diferentes.
Por exemplo, as bandas fracas no espectro por transmissão aparecerão
mais fortes na refletância.
Postado por DANIELA VINHAS.