Interpretação de espectros
Um espectrômetro de infravermelho determina as posições e
intensidades relativas de todas as absorções, ou picos, na região do IV e os
registra na forma de um espectro de IV. O espectro de IV é o gráfico de intensidade absorção versus número de onda.
Ao analisar um espectro além das posições das absorções devemos
observar as formas e intensidades dos picos. Para extrair informações estruturais do espectro usamos as Tabelas de Correlação no IV, que oferecem o máximo de informação conhecida sobre onde os
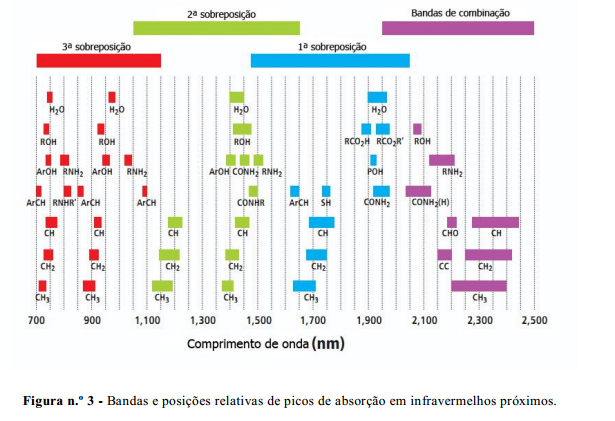
vários grupos funcionais absorvem. A figura abaixo mostra uma panorâmica das faixas de frequências
usualmente observadas para vibrações fundamental do tipo deformação angular e
estiramento de diferentes ligações químicas numa molécula orgânica.
Os tipos fundamentais de vibração molecular (estiramentos e deformações angulares) absorvem a energia da radiação eletromagnética IV em distintas regiões de freqüência. Deste modo, para efeitos de interpretação o espectro de IV pode ser dividido em três regiões:
a) Região dos Grupos Funcionais (4000 cm-1
a 1200 cm-1).
Esta é a região onde ocorre a maioria das vibrações de estiramento das ligações mais representativas dos grupos funcionais das moléculas orgânicas. Podemos determinar a presença ou ausência de grupos funcionais analisando essas frequências de absorção.
b) Região da Impressão Digital (fingerprint) da molécula (1300 cm-1
a 900 cm-1).
São absorções características das deformações angulares. Essa região do espectro é bastante complexa por apresentar um grande número de bandas de absorção, tal que cada molécula apresenta um
padrão de absorção característico e único, como se fosse uma impressão digital da substância. Devido esta complexidade fica muito difícil identificar todas as bandas de absorção.
c) Região das deformações angulares fora do plano.
É representada principalmente pela faixa de freqüência que vai de 400 cm-1 a aproximadamente 1000 cm-1.Esta região é muito útil no diagnóstico de alcenos e arenos.
Postado por: Elivânia Alexandrino Castro Silva